공부중
에너지 본문
이온화 에너지(ionization energy)
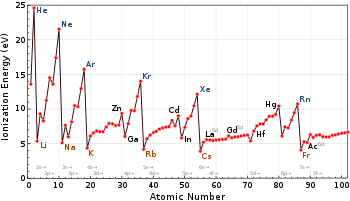
같은 족에서 원자번호가 커질수록 이온화에너지 감소
유효핵전하(effective nuclear charge)
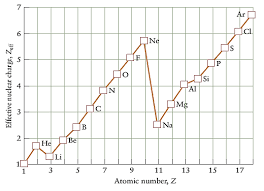
같은 족에서 원자번호 커질 수록 유효 핵전하 증가
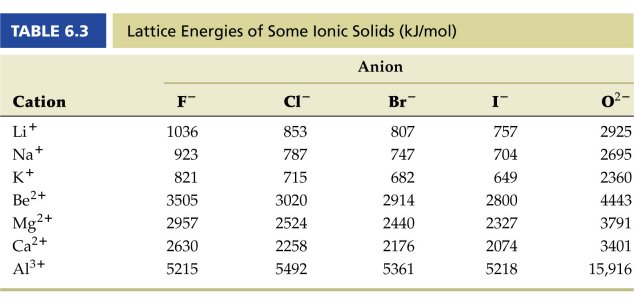
격자 에너지(lattice energy): 결정 격자에서 이온을 함께 붙잡고 있는 에너지
(= 두 이온이 결합하여 이온성 결정이 될 때 방출하는 에너지
=기체 상태의 양이온과 음이온이 만나서 고체 상태의 이온결정이 될 때의 방출하는 에너지)
- 이온의 전하가 클 수록, 중심 이온 사이의 거리가 작을 수록 커진다. (이온간 거리 :Li+<Na+<K+, 격자에너지:Li+>Na+>K+)

수화에너지
-전하가 클 수록, 원자반지름이 작을 수록 커진다.
알칼리 토금속 수산화물의 경우
원자번호가 커질 수록 격자에너지가 작아진다(이온 반지름이 증가해서)
격자 에너지 감소가 수화에너지 감소보다 큰 영향 미친다.따라서 원자번호 커질 수록 용해 잘된다.
알칼리 토금속의 황산화물의 경우
수화에너지가 용해도 경향성 지배. 원자번호 커질 수록 수화에너지가 감소해서 (원자 반지름 커진다. 둘러싸기 힘들다)용해 잘 안된다.
//할로젠분자
결합엔탈피: 일반적으로 원자번호 작을수록 핵 간 거리가 작아 결합엔탈피 커진다.
그러나 F는 크기가 작아 F2에서 고립전자쌍 사이의 반발력이 매우 커서 결합엔탈피가 비정상적으로 작다

전자친화도: 원자번호가 작을수록 전자 친화도 커진다. 그러나 그러나 F는 크기가 작아 2p 궤도 함수가 비정상적으로 큰 전자 반발력을 가진다.
격자에너지: 동일한 구조의 결정구조를 가질때는 Madelung 상수 M 큰 차이 없다.
이온간 거리가 가까울 수록 격자 에너지 크기 증가한다.

끓는점

'화학 > 일반화학' 카테고리의 다른 글
| 완충용액 (0) | 2022.06.30 |
|---|---|
| 르샤틀리에 원리 (0) | 2022.06.30 |
| 화학결합과 분자구조 (0) | 2022.05.31 |
| 전차 친화도(electron affinity) (0) | 2022.05.28 |
| 오비탈 (0) | 2022.05.28 |




